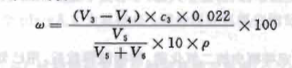GBT 4928-2008 啤酒分析方法
目录
总则
- 本标准中所采用的名词术语、计量单位应符合国家相关标准规定
- 本标准中所用的各种分析仪器(如:分析天平、分光光度计等)应定期检定;所用的密度瓶、移液管、容量瓶等玻璃计量器具应按有关检定规程进行校正。
- 本标准中所用的水,在未注明其他要求时,应符合GBT 6682-2008 分析实验室用水规格和试验方法的要求。所用试剂,在未注明其他规格时,均指分析纯(AR)。
- 本标准中的“溶液”,除另有说明外,均指水溶液。
- 同一检测项目,有两个或两个以上分析方法时,各实验室可根据各自条件选用,但以第一法为仲裁法。
试样的制备(理化分析用)及无菌采样(微生物检验用)
4.1.试样的制备
- 方法提要
- 在保证样品有代表性,不损失或少损失酒精的前提下,用振摇、超声波或搅拌等方式除去酒样中的二氧化碳气体。
- 第一法
- 将恒温至15℃~20℃的酒样约300ml倒入1000ml锥形瓶中,盖塞(橡皮塞),在恒温室内,经轻摇动、开塞放弃(开始有“砰砰”声),盖塞。反复操作,至少无气体逸出为止。用单层中速干滤纸(漏斗上面盖表面玻璃)过滤。
- 第二法
- 采用超声波或磁力搅拌法除气,将恒温至15℃~20℃的酒样约300ml移入带排气塞的瓶中,置于超声波水槽中(或搅拌器上),超声(或搅拌)一定时间后,用单层中速干滤纸(漏斗上面盖表面玻璃)过滤。
注:要通过与第一法比较,使其酒精度测定结果相似,以确定超声(或搅拌)时间和温度。
- 试样的保存
- 将除气后的酒样收集与具塞锥形瓶中,温度保持在15℃~20℃,密封保存,限制在2h内使用。
成品酒无菌采样
- 听装啤酒采样时,先将拉盖器部位浸入75%乙醇1min后,用火灼烧。再用75%乙醇棉球擦洗听顶部,并用火灼烧残余乙醇(拉盖式的听装酒,也可从另一端采样,同样无菌处理)。开盖后用无菌培养皿(或塞)盖上(或塞上)。
- 瓶装啤酒采样时,先将瓶盖器部位浸入75%乙醇1min后,用火灼烧残余乙醇。开盖后,用火灼烧瓶口,再用原盖盖住(或用消毒的铝片盖住)。
- 桶装或大罐无菌采样:预先对桶或罐取样口进行无菌处理。然后安全打开阀门,让酒液从采样器或采样口流出5s~10s,用无菌技术将样品收集于无菌瓶中。
在采样过程中,任何开盖器或采样容器都应经过灭菌处理。
感官分析
酒样的准备
根据需要将酒样密码编号并恒温至12℃~15℃,以同样高度(距杯口3cm)和注流速度,对号注入洁净、干燥的啤酒评酒杯中。
外观
- 透明度
- 将注入杯的酒样(或瓶装酒样)置于明亮处观察,记录酒的清亮程度、悬浮物及沉淀物情况。
- 浊度
- 按下面“浊度”章节测定。
泡沫
- 形态
- 用眼观察泡沫的颜色、细腻程度及挂杯情况,作好记录。
- 泡持性
- 按下面“泡持性”章节测定。
香气和口味
- 香气
- 先将注入酒样的啤酒杯置于鼻孔下方,嗅闻其香气,摇动酒杯后,再嗅闻有无酒花香气及异杂气味,作好记录。
- 口味
- 饮入适量酒样,根据所评定的酒样应具备的口感特征进行评定,做好记录。
判定
根据外观、泡沫、香气和口味特征,写出评语,依据GB 4927-2008 啤酒中的感官要求进行综合评定。
色度
- 比色计法(第一法)
- 原理
- 将除气后的试样注入EBC比色计的比色皿中,与标准EBC色盘比较,目视读取或自动数字显示出试样的色度,以色度单位EBC表示。
- 仪器
- EBC比色计(或使用同等分析效果的仪器):具有2EBC~27EBC单位的目视色度盘或自动数据处理与现实装置。
- 试剂和溶液
- 哈同(Hartong)基准溶液:称取重铬酸钾(K2Cr2O7)0.1g(精确至0.001g)和亚硝酰铁氰化钠(Na2[Fe(CN)5NO]·2H2O)3.5g(精确至0.001g),用水溶解并定容至1000ml,贮于棕色瓶中,于暗处放置24h后使用。
- 分析步骤
- 仪器校正:将哈同溶液注入40mm比色皿中,用色度计测定。其标准色度应为15EBC单位;若使用25mm比色皿,其标准色度为9.4EBC。仪器的校正应每月一次。
- 测定:将试样(4.1)注入25mm比色皿中,然后放到比色盒中,与标准色盘进行比较,当两者色调一致时直接读数。或使用自动数字显示色度计,自动显示、打印其结果。
- 结果计算
- 试样的色度按下式计算。如使用其他规格的比色皿,则需要换算成25mm比色皿的数据,计算其结果。
- 测定浓色和黑色啤酒时,需要将酒样稀释至合适的倍数,然后将测定结果乘以稀释倍数。
- 所得结果表示至一位小数。
- 精密度
- 在重复性条件下获得的两次独立测定值之差,色度为2EBC~10EBC时,不得大于0.5EBC。色度大于10EBC时,稀释样平行测定值之差不得大于1EBC。
- 分光光度计法(第二法)
- 原理
- 啤酒的色泽越深,则在一定波长下的吸光值越大,因此可直接测定吸光度,然后转换为EBC单位表示色度。
- 仪器
- 可见光光度计。
- 玻璃比色皿:10mm。
- 离心机:4000r/min。
- 分析步骤
- 将试样(4.1)注入10mm玻璃比色皿中,以水为空白调整零点,分别在波长430nm和700nm处测定试样的吸光度。
- 若A430×0.039>A700表示试样是透明的,按下面“结果计算中”的式子计算。若A430×0.039<A700表示试样是浑浊的,需要离心或过滤后,重新测定。当A430的吸光度值在0.8以上时,需用水稀释后,再测定。
- 精密度
- 在重复性条件下获得的两次独立测定值之差,不得大于0.5EBC。
浊度
原理
利用福尔马肼(Formazin)标准浊度溶液矫正浊度计,直接测定啤酒样品的浊度,以浊度单位EBC表示。
仪器
- 浊度计:测量范围0EBC~5EBC,分度值0.01EBC。
- 分析天平:感量0.1mg。
- 具塞锥形瓶:100ml。
- 吸管:25ml。
试剂和溶液
- 硫酸肼溶液(10g/L):称取硫酸肼1g(精确至0.001g),加水溶解,并定容至100ml。静置4h使其完全溶解。
- 六次甲基四胺溶液(100g/L):称取六次甲基四胺10g(精确至0.001g),加水溶解,并定容至100ml。
- 福尔马肼标准浊度储备液:吸取25.0ml六次甲基四胺溶液于一个具塞锥形瓶中,边搅拌边用吸管加入25.0ml硫酸肼溶液,摇匀,盖塞,于室温下放置24h后使用。此溶液为1000EBC单位,在2个月内可保持稳定。
- 福尔马肼标准浊度使用液:分别吸取标准浊度储备液0ml、0.20ml、0.50ml、1.00ml于4个1000ml容量瓶中,加重蒸水稀释至刻度,摇匀。该标准浊度使用液的浊度分别为0EBC、0.20EBC、0.50EBC、1.00EBC。该溶液应当天配置与使用。
分析步骤
- 按照仪器使用说明书安装与调试。用标准浊度使用液矫正浊度计。
- 取按4.1除气但未经过滤,温度在20℃±0.1℃的试样倒入浊度计的标准杯中,将其放入浊度计中测定,直接读数(该法为第一法,应在试样脱气候5min内测定完毕)。
- 或者将整平酒放入仪器中,旋转一周,取平均值(该法为第二法,预先在瓶盖上划一个十字,手工旋转四个90°,读数,取四个读数的平均值报告其结果)。
- 所得结果表示至一位小数。
精密度
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。
泡持性
仪器法(第一法)
- 原理
- 采用节流发泡,利用泡沫的导电性,使用长短不同的探针电极,自动跟踪记录泡沫衰减所需的时间,即为泡持性。
- 仪器和材料
- 啤酒泡持鉴定仪。
- 泡持杯:杯内高120mm,内径60mm,壁厚2mm,无色透明玻璃。
- 气源:液体二氧化碳,钢瓶压力P≥5MPa,纯度≥99%。
- 恒温水浴:精度±0.5℃。
- 分析步骤
- 7.1.3.1.试样的准备
- 将酒样(整瓶或整听)置于20℃±0.5℃水浴中恒温30min。
- 将泡持杯彻底清洗干净、备用。
- 测定
- 按使用说明书调试仪器至工作状态。
- 将二氧化碳钢瓶分压调至0.2MPa。按仪器说明书校正杯高。
- 按照仪器使用说明书将样品置于发泡器上发泡。泡沫出口端与泡持杯底距离10mm,泡沫满杯时间宜为3s~4s。
- 迅速将盛满泡沫的泡持杯置于泡沫测量仪的探针下,按开始键,仪器自动显示和记录结果。
- 所得结果表示至整数。
- 精密度
- 在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的5%。
秒表法(第二法)
- 原理
- 用目视法测定啤酒泡沫消失的速度,以秒表示。
- 仪器和材料
- 秒表。
- 泡持杯:杯内高120mm,内径60mm,壁厚2mm,无色透明玻璃。
- 铁架台和铁环。
- 分析步骤
- 试样的准备
- 同7.1.3.1。
- 测定
- 将泡持杯置于铁架台底座上,距杯口3cm处固定铁环,开启瓶盖,立即置瓶(或听)口于铁环上,沿杯中心线,以均匀流速将酒样注入杯中,直至泡沫高度与杯口相齐时为止(满杯时间宜控制在4s~8s内)。同时按秒表开始计时。
- 观察泡沫升起情况,记录泡沫的形态(包括色泽及细腻程度)和泡沫挂杯情况。
- 记录泡沫从满杯至消失(露出0.05cm2酒面)的时间。
- 测定时严禁有空气流通,测定前样品瓶应避免振摇。
- 所得结果表示至整数。
- 精密度
- 在重复性条件下获得的两次毒力测定结果的绝对差值不得超过算术平均值的10%。
酒精度
密度瓶法(第一法)
- 原理
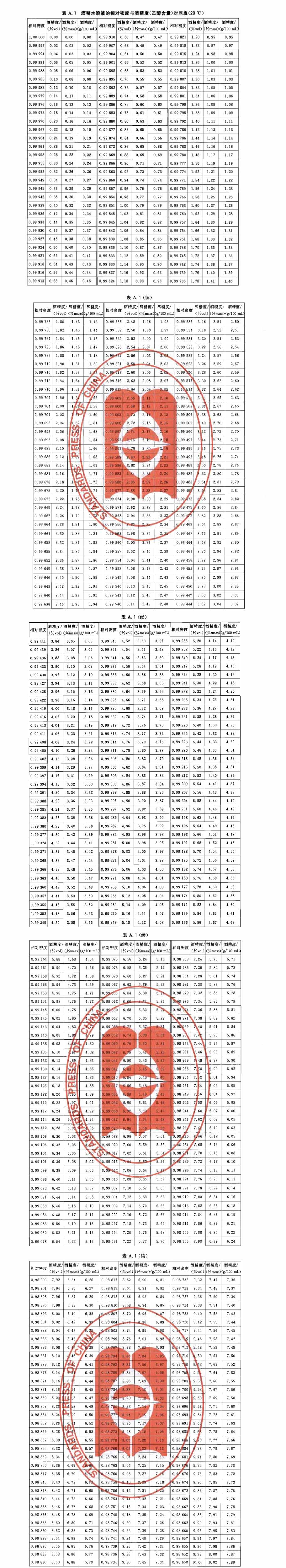
- 利用在20℃时酒精水溶液与同体积纯水质量之比,求得相对密度。然后,查表得出试样中酒精含量的体积分数。
- 8.1.2.仪器
- 全玻璃整流器:500ml。
- 恒温水浴:精度±0.1℃。
- 容量瓶:100ml。
- 移液管:100ml。
- 分析天平:感量0.1mg。
- 天平:感量0.1g。
- 附温度计密度瓶:25ml或50ml。
- 分析步骤
- 8.1.3.1.容量法
- 蒸馏
- 用100ml容量瓶准确量取试样(4.1)100ml,置于蒸馏瓶中,用50ml水分三次冲洗容量瓶,洗液并入蒸馏瓶中,加玻璃珠数粒,装上蛇形冷凝管,用原100ml容量瓶接收馏出液(外加冰浴),换换加热蒸馏(冷凝管出口水温不得超过20℃),收集约96ml馏出液(蒸馏应在30min~60min内完成),取下容量瓶,调节液温至20℃,补加水定容,混匀,备用。
- 测量A
- 将密度瓶洗净、干燥、称量,反复操作,直至恒重。将煮沸冷却至15℃的水注满恒重的密度瓶中,插上温度计的瓶塞(瓶中应无气泡),立即浸于20℃±0.1℃的水浴中,待内容物温度达20℃,并保持5min不变后取出。用滤纸吸去溢出支管的水,立即盖好小帽,擦干后,称量。
- 测量B
- 将水倒去,用试样馏出液反复冲洗密度瓶三次,然后装满,按测量A同样操作。
- 计算
- 试样馏出液(20℃)的相对密度按下式计算:
- 8.1.3.2.重量法
- 蒸馏
- 称取试样(4.1)100g(精确至0.1g),全部移入500ml已知质量的蒸馏瓶中,加水50ml和数粒玻璃珠,装上蛇形冷凝器(或冷却部分的长度不短于400mm的直型冷凝器),开启冷却水,用已知质量的10ml容量瓶接收馏出液(外加冰浴),换换加热蒸馏(冷凝管出口水温不得超过20℃),收集约96ml馏出液(蒸馏应在30min~60min内完成),取下容量瓶,调液温至20℃,然后补加水,使馏出液质量为100.0g(此时总质量为100.0g+容量瓶质量),混匀(注意保存蒸馏后的残液,可供做真正浓度用)。
- 测量A和测量B
- 同上面“容量法”
- 试样馏出液(20℃)相对密度的计算
- 同上面“容量法”
- 根据相对密度查附表A,得到试样馏出液的酒精含量的质量分数,即试样的酒精度。
- 所得结果表示至一位小数。
- 8.1.4.精密度
- 在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的1%。
气相色谱法(第二法)
- 原理
- 试样进入气相色谱仪中的色谱柱时,由于在气固两相中吸附系数不同,而使乙醇与其他组分得以分离,利用氢火焰离子化检测器进行检测,与标样对照,根据保留时间定性,利用内标法定量。
- 仪器
- 气相色谱仪:配有FID检测器。
- 微量注射器:1μL。
- 试剂和材料
- 8.2.3.1.乙醇标准溶液:用乙醇(色谱纯)配制成2%、3%、4%、5%、6%、7%(体积分数)的乙醇标准溶液。
- 8.2.3.2.正丁醇:色谱纯,做内标用。
- 色谱柱与色谱条件
- 色谱柱(不锈钢或玻璃):2m;或使用同等分析效果的其他色谱柱。
- 固定相:Chrornosorb 103,60目~80目。
- 柱温:200℃。
- 气化室和检测器温:240℃。
- 载气(高纯氮)流量:40ml/min。
- 氢气流量:40ml/min。
- 空气流量:500ml/min。
- 应根据不同仪器,通过实验选择最佳色谱条件,以使乙醇和正丁醇获得完全分离,并使乙醇洗脱时间控制在1min,正丁醇(内标)在1.6min为最佳。
- 分析步骤
- 8.2.5.1.工作曲线的绘制
- 分别吸取不同浓度的乙醇标准溶液(8.2.3.1)各10.0ml于5个10ml容量瓶中,分别加入0.50ml正丁醇(8.2.3.2),混匀。在上述色谱条件下,进样0.3μL,以标样和内标峰面积的比值(或峰高比值),对应酒精度绘制工作曲线,或建立相应的回归方程。
- 注:所用乙醇标准溶液应当天配置与使用,每个浓度至少要做两次,取平均值作图或计算。
- 试样的测定
- 吸取试样(4.1)10.0ml于10ml容量瓶中,加入0.5ml正丁醇(8.2.3.2),混匀。以下色谱分析操作同8.2.5.1。
- 结果计算
- 用试样的乙醇峰面积与内标峰面积的比值(或峰高比值),查工作曲线,或用回归方程计算出试样的酒精度,%vol。
- 所得结果表示至一位小数。
- 精密度
- 同8.1.4。
仪器法(第三法)
- 原理
- 除气后的啤酒试样倒入啤酒自动分析仪后,一路进入内部组装的“U”形震荡管密度计中,测定其密度;另一路进入酒精传感器,测定啤酒试样中的酒精度。
- 仪器
- 啤酒自动分析仪:酒精度分析精度0.02%;或使用同等分析效果的仪器,并按其仪器说明书进行操作。
- 容量瓶:1L。
- 试剂和溶液
- 乙醇(95)。
- 清洗液:按仪器使用说明书配置。
- 乙醇校准溶液(3.5% mass):取量95%乙醇46ml,加水定容至1L。
- 乙醇校准溶液(7.0% mass):取量95%乙醇91ml,加水定容至1L。
- 分析步骤
- 按啤酒自动分析仪使用说明书安装与调试仪器。
- 按啤酒自动分析仪使用手册,依次用水、3.5%乙醇校准溶液和7.0%乙醇校准溶液矫正仪器。
- 将试样(4.1)导入啤酒自动分析仪进行测定。
- 结果计算
- 仪器自动打印酒精度,以体积分数%vol或质量分数%mass表示。
- 所得结果表示至一位小数。
- 精密度
- 同8.1.4。
原麦汁浓度
原理
以密度瓶法测出啤酒样式中的真正浓度和酒精度。按经验公式计算出啤酒试样的原麦汁浓度。或用仪器法直接自动测定、计算、打印出试样的真正浓度及原麦汁浓度。
密度瓶法(第一法)
- 真正浓度的测定
- 仪器
- 同8.1.2。
- 分析步骤
- 试样的制备
- 将在8.1.3.2蒸馏除去酒精后的残液(在已知质量的蒸馏烧瓶中),冷却至20℃,准确补加水使残液至100.0g,混匀。或用已知质量的蒸发皿称取试样(4.1)100.0g(精确至0.1g),于沸水浴上蒸发,直至原体积的三分之一,取下冷却至20℃,加水恢复至原质量,混匀。
- 测定
- 用密度瓶或密度计测定出残液的相对密度。查附录B中的表B.1,求得100g试样中浸出物的克数(g/100g)。即为啤酒的真正浓度,以柏拉图度或质量分数(°P或%)表示。
- 酒精度的测定
- 同8.1.3.2。
- 结果计算
- 精密度
- 在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的1%。
仪器法(第二法)
- 仪器
- 啤酒自动分析仪(或使用同等分析效果的仪器):真正浓度分析精度0.01%。
- 分析步骤
- 按啤酒自动分析仪使用说明书安装与调试仪器。
- 按仪器使用手册的进行操作,自动进样、测定、计算、打印出试样的真正浓度和原麦汁浓度,以柏拉图度或质量分数(°P或%)表示。
- 所得结果表示至一位小数。
- 精密度
- 在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的1%。
总酸
电位滴定法(第一法)
- 原理
- 酸碱中和原理。用氢氧化钠标准溶液直接滴定啤酒试样中的总酸,以pH=8.2为电位滴定终点,根据消耗氢氧化钠标准溶液的体积计算出啤酒中总酸的含量。
- 仪器
- 自动电位滴定仪:精度±0.02,附电磁搅拌器。
- 恒温水浴:精度±0.5℃,带振荡装置。
- 试剂和溶液
- 10.1.3.1.氢氧化钠标准滴定溶液[c(NaOH)=0.1mol/L]:按GBT 601-2002 化学试剂 标准滴定溶液的制备配置与标定。
- 标准缓冲液:现用现配。
- 分析步骤
- 10.1.4.1.试样的准备
- 取试样(4.1)约100ml于250ml烧杯中,置于40℃±0.5℃振荡水浴中恒温30min,取出,冷却至室温。
- 测定
- 按仪器使用说明书安装与调试仪器。
- 用标准缓冲溶液校正自动电位滴定仪。用水清洗电极,并用滤纸吸干附着电极的液珠。
- 吸取试样(10.1.4.1)50.0ml与烧杯中,插入电极,开启电磁搅拌器,用氢氧化钠标准滴定溶液(10.1.3.1)滴定至pH=8.2为其终点,记录消耗氢氧化钠标准溶液的体积。
- 结果计算
- 试样的总酸含量(即100ml试样消耗氢氧化钠标准滴定溶液(c(NaOH)=1.0mol/L)的毫升数)按下式计算:
- X2 = 2×c1×V1
- 式中:
- X2——试样的总酸含量,单位为毫升每百毫升(ml/100ml);
- c1——氢氧化钠标准滴定溶液的浓度,单位为摩尔每升(mol/L);
- V1——消耗氢氧化钠标准滴定溶液的体积,单位为毫升(ml);
- 2——换算成100ml试样的系数。
- 所得结果表示至一位小数。
- 10.1.6.精密度
- 在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的4%。
指示剂法(第二法)
- 原理
- 用酚酞做指示剂进行酸碱中和滴定。
- 仪器
- 锥形瓶:250ml。
- 移液管:10ml。
- 滴定管。
- 试剂和溶液
- 酚酞指示液(5g/L):按GBT 603-2002 化学试剂 试验方法中所用制剂及制品的制备配置。
- 10.2.3.2.氢氧化钠标准滴定溶液[c(NaOH)=0.1mol/L]:按GBT 601-2002 化学试剂 标准滴定溶液的制备配置与标定。
- 分析步骤
- 于250ml锥形瓶中装入100ml水,加热煮沸2min。然后加入试样(4.1)10.0ml,继续加热1min,控制加热温度使其在最后30s内再次煮沸。放置5min后,用自来水迅速冲冷盛样的锥形瓶至室温。加入0.50ml酚酞指示液,用氢氧化钠标准滴定溶液(10.2.3.2)滴定至淡粉色为其终点。记录消耗氢氧化钠标准滴定溶液的体积。
- 结果计算
- 试样的总酸含量(即100ml试样消耗氢氧化钠标准滴定溶液(c(NaOH)=1.0mol/L)的毫升数),按下式计算:
- X3=10×c2×V2
- 式中:
- X3——试样的总酸含量,单位为毫升每百毫升(ml/100ml);
- c2——氢氧化钠标准滴定溶液的浓度,单位为摩尔每升(mol/L);
- V2——消耗氢氧化钠标准滴定溶液的体积,单位为毫升(ml);
- 10——换算成100ml试样的系数。
- 所得结果表示至一位小数。
- 精密度
- 同10.1.6。
二氧化碳
标准法(第一法)
- 原理
- 在0℃~5℃下用碱液固定啤酒中的二氧化碳,加稀酸释放后,用已知量的氢氧化钡溶液吸收,过量的氢氧化钡溶液再用盐酸标准滴定溶液滴定。根据消耗盐酸标准滴定溶液的体积,计算出试样中二氧化碳的含量。
- 仪器
- 二氧化碳收集测定仪。
- 锥形瓶:150ml。
- 酸式滴定管:25ml。
- 试剂和溶液
- 无二氧化碳蒸馏水:按GBT 603-2002 化学试剂 试验方法中所用制剂及制品的制备制备。
- 碳酸钠:国家二级标准物质GBW(E) 060023(无水碳酸钠纯度标准物质,无水碳酸钠纯度99.95%,相对10-2)。
- 11.1.3.3.氢氧化钠溶液(300g/L):称取300g氢氧化钠,用水溶解,并定容至1L。
- 酚酞指示液(10g/L):按GBT 603-2002 化学试剂 试验方法中所用制剂及制品的制备制备。
- 盐酸标准滴定溶液(c(HCl)=0.1mol/L):按GBT 601-2002 化学试剂 标准滴定溶液的制备配制与标定。
- 11.1.3.6.氢氧化钡溶液(0.055mol/L)
- 配制:称取氢氧化钡19.2g,加无二氧化碳蒸馏水600ml~700ml,不断搅拌直至溶解,静置24h。加入氯化钡29.2g,搅拌30min,用无二氧化碳蒸馏水定容至1000ml。静置沉淀后,过滤于一个密闭的试剂瓶中,贮存备用。
- 标定:吸取上述溶液25.0ml于150ml锥形瓶中,加酚酞指示液两滴,用盐酸标准滴定溶液滴定至刚好无色为其终点,记录消耗盐酸标准滴定溶液的体积(该值应在27.5ml~29.5ml之间,若超出30ml,应重新调整氢氧化钡溶液的浓度)。在密封良好的情况下贮存(试剂瓶顶端装有钠石灰管,并附有25ml加溶液)。若盐酸标准溶液滴定浓度不变,可连续使用一周。
- 11.1.3.7.硫酸溶液(10%(质量分数))。
- 11.1.3.8.有机硅消泡剂(二甘油聚醚)。
- 分析步骤
- 仪器的校正
- 按仪器使用说明书,用碳酸钠标准物质校正仪器。每季度校正一次(发现异常亦应校正)。
- 11.1.4.2.试样的准备
- 将待测啤酒恒温至0℃~5℃。瓶装酒开启瓶盖,迅速加入一定量的氢氧化钠溶液(11.1.3.3)和消泡剂(11.1.3.8)2滴~3滴,立刻用塞塞紧,摇匀,备用。听装酒可在罐底部打孔,按瓶装酒同样操作。
- 注:氢氧化钠溶液添加量,样品净含量为640ml时,加10ml;355ml时,加5ml;2L时,加25ml。
- 测定
- 二氧化碳的分离与收集:吸取试样(11.1.4.2)10.0ml于反应瓶中,在收集瓶中加入25.0ml氢氧化钡溶液(11.1.3.6);将收集瓶与仪器的分气管接通。通过反应瓶上分液漏斗向其中加入10ml硫酸溶液(11.1.3.7),关闭漏斗活塞,迅速接通连接管,设定分离与收集时间10min,按下泵开关,仪器开始工作,直至自动停止。
- 滴定:用少量无二氧化碳蒸馏水冲洗收集瓶的分气管,取下收集瓶,加入酚酞指示液两滴,用盐酸标准滴定溶液滴定至刚好无色,记录消耗盐酸标准滴定溶液的体积。
- 试样的净含量按15.1测定。
- 试样的相对密度,按8.1.3.1的方法测定或用数字密度计测量。
- 结果计算
- 式中:
- ω——试样的二氧化碳质量分数,%;
- V3——标定氢氧化钡溶液时,消耗的盐酸标准滴定溶液的体积,单位为毫升(ml);
- V4——试样消耗盐酸标准滴定溶液的体积,单位为毫升(ml);
- c3——盐酸标准滴定溶液的浓度,单位为摩尔每升(mol/L);
- 0.022——与1.00ml盐酸标准溶液(c(HCl)=1.000mol/L)相当的以克表示的二氧化碳的质量,单位为克(g);
- V5——试样的净含量(总体积),单位为毫升(ml);
- V6——在试样准备时,加入氢氧化钠溶液的体积,单位为毫升(ml);
- 10——测定时吸取试样的体积,单位为毫升(ml);
- ρ——被测试样的密度(当被测试样的原麦汁浓度为11°P或12°P时,此值为1.012,其他浓度的试样需先测其密度),单位为克每毫升(g/ml)。
- 所得结果表示至两位小数。
- 精密度
- 在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的5%。
压力法(第二法)
- 原理
- 根据亨利定律,在25℃时用二氧化碳压力测定仪测出试样的总压、瓶颈空气体积和瓶颈空容体积,然后计算出啤酒中二氧化碳的含量。
- 仪器
- 二氧化碳测定仪:压力表的分度值为0.01MPa。
- 分析天平:感量0.1g。
- 玻璃铅笔(或记号笔)。
- 11.2.3.试剂和溶液
- 氢氧化钠溶液(400mlg/L):称取400g氢氧化钠,用水溶解,并定容至1L。
- 分析步骤
- 仪器的准备
- 将二氧化碳测定仪的三个组成部分之间用胶管(或塑料管)接好,在碱液水准瓶和刻度吸管中装入氢氧化钠溶液(11.2.3),用水或氢氧化钠溶液(可也以使用瓶装酒)完全顶出链接刻度吸收管与穿孔装置之间胶管中的空气。
- 11.2.4.2.试样的准备
- 取瓶(或听)装啤酒样置于25℃水浴中恒温30min。
- 测表压
- 将试样(11.2.4.2)酒瓶(或听)置于穿孔装置下穿孔。用手摇动酒瓶(或听)直至压力表指针达到最大恒定值,记录读数(即表压)。
- 测瓶颈空气
- 慢慢打开穿孔装置的出口阀,让瓶(或听)内气体缓缓流入吸收管,当压力表指示降至零时,立即关闭出口阀,倾斜摇动吸收管,直至气体体积达到最小恒定值。调整水准瓶,使之静压箱等,从刻度吸收管上读取气体的体积。
- 测瓶颈空容
- 在测定前,先在酒的瓶壁上用玻璃铅笔标记出酒的液面。测定后,用水将酒瓶装满至标记处,用100ml量筒量取100ml水后倒入试样瓶至满瓶口,读取从量筒倒出水的体积。
- 听(铝易开盖两片罐)装酒“听顶空容”的测定与计算
- 在测定前,先称量整听酒的质量(m3),精确至0.1g;穿刺,测定听装酒的表压;将听内啤酒倒出,用水洗净,控干,称量“听+拉盖”的质量(m4),精确至0.1g;再用水充满空听,称量“听+拉盖+水”的质量(m5),精确至0.1g。
- 结果计算
- 精密度
- 在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的5%。
双乙酰
原理
用蒸汽将双乙酰蒸馏出来,与邻苯二胺反应,生成2,3-二甲基喹喔啉,在波长335nm下测其吸光度。由于其他连二酮类都具有相同的反应特性,另外蒸馏过程中部分前驱体要转化成连二酮,因此上述测定结果为总连二酮含量(以双乙酰表示)。
仪器
- 带有加热套管的双乙酰蒸馏器。
- 蒸汽发生瓶:2000ml(或3000ml)锥形瓶或平底蒸馏烧瓶。
- 容量瓶:25ml。
- 紫外分光光度计:备有20mm石英比色皿或10mm石英比色皿。
试剂和溶液
- 12.3.1.盐酸溶液(4mol/L):按GBT 601-2002 化学试剂 标准滴定溶液的制备配置。
- 邻苯二胺溶液(10g/L):称取邻苯二胺0.100g,用盐酸溶液(12.3.1)溶解,并定容至10ml,摇匀,放于暗处。此溶液须当天配制与使用;若配制出来的溶液呈红色,应重新更换。
- 有机硅消泡剂(或甘油聚醚)。
分析步骤
- 蒸馏
- 将双乙酰蒸馏器安装好,加热蒸汽发生瓶至沸。通汽预热后,置25ml容量瓶于冷凝器出口接收馏出液(外加冰浴),加1滴~2滴消泡剂于100ml量筒中,再注入未经除气的预先冷至5℃的酒样100ml,迅速转移至蒸馏器内,并用少量水冲洗带塞漏斗,盖塞。然后用水密封,进行蒸馏,直至馏出液接近25ml(蒸馏需在3min内完成)时取下容量瓶,达到室温后用重蒸水定容,摇匀。
- 显色与测量
- 分别吸取馏出液10.0ml于两支干燥的比色管中,并于第一支管中加入邻苯二胺溶液0.50ml,第二支管中不加(做空白),充分摇匀后,同时置于暗处放置20min~30min,然后于第一支管中加入2ml盐酸溶液(12.3.1),于第二支管中加入2.5ml盐酸溶液(12.3.1),混匀后,用20mm石英比色皿(或10mm石英比色皿),于波长335nm下,以空白作参比,测定其吸光度(比色测定操作需在20min内完成)。
结果计算
精密度
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。
真正(实际)发酵度
试样的真正发酵度按下式计算:
或者按下式计算:
蔗糖转化酶活性
原理
不经巴氏灭菌或高温灭菌的啤酒,酒体中各种酶系仍保持着活性,其中的蔗糖转化酶可以将蔗糖分解为葡萄糖,利用葡萄糖鉴别试纸可以检查酒体中的蔗糖转化酶活性。
仪器
- 移液管
- 试管
- 恒温水浴:温控精度±0.5℃
试剂和溶液
- 14.3.1.蔗糖溶液(250g/L):称取蔗糖25g,用水溶解,并定容至100ml。
- 葡萄糖鉴别试纸。
分析步骤
分别吸取酒样(4.1)10ml于三支试管中。于第一支试管(A)中加水2.0ml,摇匀。将第二支试管(B)置于沸水中加热2min,取出冷却。于第二支试管(B)和第三支试管(C)中各加入2.0ml蔗糖溶液(14.3.1),摇匀。然后三支试管同时置于30℃±0.5℃水浴中保温30min。随后将三支试管再同时置于沸水中加热2min,取出,冷却至室温。分别用葡萄糖鉴别试纸的一端浸入各试管中30s~60s,取出,立即观察其颜色变化,记录结果。
判定
若C管试纸变色且颜色深于A管和B管(呈阳性),则判为生啤酒或鲜啤酒。若不变色或者与A管和B管颜色无差别,则判为熟啤酒。
净含量
15.1.重量法(第一法)
- 仪器
- 分析天平:感量0.01g
- 台秤:感量0.1kg
- 恒温水浴:精度±0.5℃
- 分析步骤
- 15.1.2.1.瓶装、听(铝易开盖两片罐)装啤酒的测定
- 桶装啤酒的测定
- 桶装啤酒于室温下,用台秤称量,其余步骤同15.1.2.1.
容量法(第二法)
- 仪器
- 量筒
- 玻璃铅笔(或记号笔)
- 分析步骤
- 将瓶装酒样置于20℃±0.5℃水浴中恒温30min。取出,擦干瓶外壁的水,用玻璃铅笔对准酒的液面划出一条细线,将酒液倒出,用自来水冲洗瓶内(注意不要洗掉划线)至无泡沫为止,擦干瓶外壁的水,准确装入水至瓶划线处,然后将水倒入量筒,测量水的体积,即为瓶装啤酒的净含量。
附录 A
附录 B
糖溶液的相对密度和Plato度或浸出物的百分含量(20℃)及计算原麦汁浓度经验公式校正表

附录 C
企业自控技术指标的分析方法
保质期的预测
原理
模拟市场条件保存,定期检测非生物性浑浊度;将成品酒先后置于0℃和60℃水浴中保持一定时间,然后测定其浑浊度。
仪器
- 浊度计:测量范围0EBC~5EBC,分度值0.01EBC(带瓶检测时应排除啤酒瓶颜色干扰)。
- 恒温冷水浴:带制冷剂的可调温水浴。
- 恒温水浴:精度±1℃,配有循环装置。
取样及样品准备
- 瓶装产品,从灌装线上随机抽取样品3瓶~6瓶(为一组)。如瓶子适于测浑浊度(瓶壁光洁,色调一致,无划痕、疤疖或气泡),就不需要处理,否则需要重新取样。
- 以其他形式包装(如听装啤酒)的产品,从灌装线上随机抽取样品后,需要转移到合适的瓶子中。在换包装过程中,应注意严格排除空气。
分析步骤
- 长期保存法
- 模拟市场条件(如:温度、光照、环境等)长期保存,每两周(或一个月)定期检测非生物性浑浊度一次,做好记录,直至保存3个月~6个月。
- 快速预测法(加速浑浊试验)
- 以3瓶~6瓶酒味一组,放入0℃冷水浴24h,取出,恢复到室温用浊度计测其最初的浊度(EBC单位)。
- 将其置于恒温水浴中垂直不动,升温至60℃±1℃,放置48h(从放入恒温水浴中开始计时)。
- 再将其放入冷水浴,降温至0℃,放置24h(从放入冷水浴中开始计时)。取出,恢复到室温,用浊度计测其最终浊度(EBC单位)。
- 注1:在测定浊度时,酒瓶的合缝不能置于浊度计的光路上。
- 注2:本方法推荐采用上述循环周期,是为了不同生产厂和不同国家间的技术交流与比较。各生产厂可根据企业不同类型产品,自定周期。
苦味质
比色法
- 原理
- 用异辛烷萃取苦味质,在波长275nm下测定吸光度,计算国际通用的苦味质单位(BU)。
- 仪器
- 紫外分光光度计:备有10mm石英比色皿
- 电动振荡器:振幅20mm~30mm
- 离心机:3000r/min以上,适用于50ml离心管。
- 离心管:50ml,带玻璃塞或聚四氟乙烯旋盖
- 移液管
- 试剂和溶液
- 辛醇
- 2.1.3.2.异辛烷:在20ml异辛烷中加一滴辛醇,用10mm比色皿,在波长275nm下,测其吸光度,该吸光度应接近重蒸馏水或不高于0.005。
- 2.1.3.3.盐酸溶液(3mol/L):按GBT 601-2002 化学试剂 标准滴定溶液的制备配置。
- 分析步骤
- 用尖端带有一滴辛醇的移液管,吸取未除气的冷啤酒样(10℃)10.0ml于50ml离心管中,加1ml盐酸溶液(2.1.3.3)和20ml异辛酸(2.1.3.2),拧紧盖,置于电动振荡器上振摇15min(应呈乳状),然后移到离心机上离心10min,使其分层。尽快吸出上层液(异辛烷层),用10mm比色皿,在波长275nm下,以异辛烷(2.1.3.2)作参比液,测定其吸光度A275。
- 结果计算
- 试样的苦味质含量按下式计算:
- 精密度
- 试样的苦味质在10BU~45BU时,再现性误差的变异系数为3%。
- 注1:可用250ml具塞锥形瓶(或分液漏斗)代替离心管,向其中加几颗玻璃珠(或沸石),在电动振荡器振摇萃取,然后转入离心管离心。
- 注2:使用后的异辛烷,可以收集处理,重复使用。处理方法:加入4%的活性炭,振摇,过滤回收(或加颗粒氢氧化钠,摇动后,放置过夜),重蒸;或重蒸后,用S-156 408硅胶(12目~28目)柱处理,使馏出液的吸光度(用10mm比色皿,在波长275nm下)接近重蒸馏水或不高于0.005.
高效液相色谱法(测异α-酸)
- 原理
- 除气啤酒通过柱层析,将其中的异α-酸分离为异副葎草酮、异葎草酮和异合葎草酮,并吸附到固定相上,然后又选择的洗脱下来,用高效液相色谱仪测定。
- 仪器
- 高效液相色谱仪:带紫外检测器和数据处理装置。
- C.2.2.2.2.色谱柱:CLC-ODS,25cm×4.6mm(或同等分析效果的色谱柱)。
- C8 SPE octyl柱:500mg,3ml。
- 容量瓶:2ml、100ml。
- 移液管:20ml。
- 刻度移液管:1ml、5ml、10ml。
- 塑料注射器:30ml。
- 分析天平:感量0.1mg。
- 试剂和溶液
- 标样:已知异α-酸含量的标样,如异α-酸镁盐。
- 10%四乙胺氢氧化物水溶液(tetraethylammonium hydroxide)。
- 重蒸馏水。
- C.2.2.3.4.甲醇:色谱纯。
- C.2.2.3.5.磷酸:85%(质量分数)。
- C.2.2.3.6.SPE柱洗脱液A:水+磷酸=100+2。
- C.2.2.3.7.SPE柱洗脱液B:水+甲醇+磷酸=50+50+0.2。
- C.2.2.3.8.SPE柱洗脱液C:甲醇+磷酸=100+0.1。
- C.2.2.3.9.流动相:甲醇+重蒸水+磷酸+四乙基氢氧化胺=780ml+220ml+17g+29.5g。
- 分析步骤
- C.2.2.4.1.试样的处理
- 取试样(4.1)100ml,加磷酸(C.2.2.3.5)200μL,调节pH至约2.5。
- 吸附与解吸
- 装好C8 SPE柱后,先后用下列溶液走柱:
- 2ml甲醇(C.2.2.3.4),弃去流出液;
- 2ml重蒸水,弃去流出液;
- 20ml试样(C.2.2.4.1),弃去流出液;
- 6ml洗脱液A(C.2.2.3.6),弃去流出液;
- 2ml洗脱液B(C.2.2.3.7),弃去流出液;
- 用连续3份0.6ml洗脱液C(C.2.2.3.8)洗脱,收集流出液于2.0ml容量瓶中,用洗脱液C定容并充分混匀,作为待测试样。
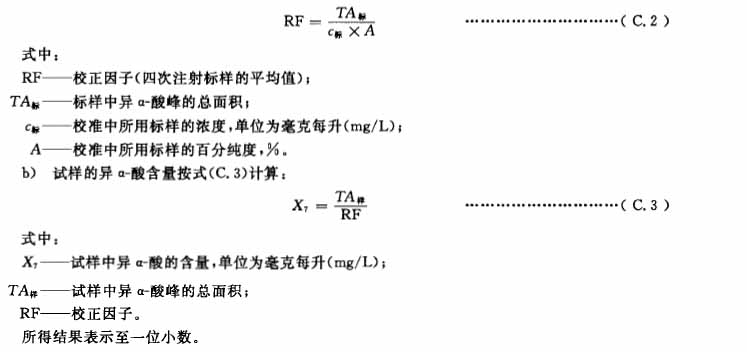
- 校准
- 称取异α-酸标样20mg(精确至0.1mg),用甲醇溶解,并定容至100ml。在测定试样前,注射标样20μL两次;在测完试样后,注射标样20μL两次,取四次校正因子的平均值。
- 待测试样的测定
- 色谱条件:
- 流速:1.0ml/min;
- 柱温:30℃;
- 检测器波长:280nm;
- 进样量:20μL。
- 将流动相(C.2.2.3.9)以流速1.0ml/min冲洗色谱柱(C.2.2.2.2)过夜(流动相可回收使用),待仪器稳定后即可进行分析,以外标法计算含量。
- 结果计算
- 精密度
- 试样中异α-酸含量在10mg/L~30mg/L时,重复性误差的变异系数为4%;再现性误差的变异系数为13%。
pH
原理
将玻璃电极和甘汞电极同时插入试样溶液中,构成一个原电池。两极间的电动势与溶液的pH值有关,通过测量原电池的电动势,即可得到试样溶液的pH值。
仪器
- 酸度计(pH计):精度±0.02,带磁力搅拌装置。
- 烧杯:50ml。
试剂和溶液
缓冲溶液按GBT 603-2002 化学试剂 试验方法中所用制剂及制品的制备配制,如使用商品缓冲剂时,应是新配制的(已发霉或有沉淀的缓冲液不得使用)。
分析步骤
- 按仪器使用说明书安装。
- 按仪器使用说明书校准。
- 在室温下,取试样(4.1)50ml于烧杯中,将电极插入试样液中,待pH稳定后读书(测定样品后,电极应尽快用水冲洗,吸干)。
- 所得结果表示至一位小数。
精密度
试样的pH平均值为4.25时,再现性误差的变异系数为1.5%。
溶解氧(仪器法)
原理
从啤酒包装物(瓶装酒的顶部或听装酒的底部)穿刺,将取样管插入样液中,利用惰性气体(如:二氧化碳或高纯氮气)将啤酒样液顶入装有氧传感器的流通池中,测量其样液中的溶解氧含量。
仪器
- 溶解氧分析仪:如奥比菲亚实验室仪器(或使用同等分析效果仪器)。
- 气源:二氧化碳或高纯氮气,纯度99.99%以上。
分析步骤
- 按仪器说明书进行安装与调试。
- 接通电源,打开显示器。按仪器使用说明书操作。将瓶(或听)装酒样放到仪器取样器下,调整取样器的高度,穿刺后压下取样针,使其伸入到(距瓶、听底三分之一处)样液里。打开气源,调节酒液流速约200ml/min,使稳定,连续的酒样流出,待数值稳定后读数。
- 注全部样品测定完后,关掉显示器,应及时清洗。取一干净的啤酒瓶装满水,重复上述操作,清洗整个流通系统。在取样针露出液面之前,提起取样针,关掉减压阀,使操纵杆复位,关闭二氧化碳总阀和电源。将仪器擦拭干净。
- 所得结果表示至整数。
精密度
试样的溶解氧平均值为400μg/L时,再现性误差的变异系数为8%。
蛋白质
原理
在催化剂作用下,用硫酸分解样品,使有机化合物中的氮转变成氨,以硼酸溶液吸收蒸馏出的氨,用酸碱滴定法测定氮含量。
仪器
- 凯氏定氮仪:自行组装的仪器或成套仪器。
- 分析天平:感量0.1mg。
- 滴定管:50ml。
- 锥形瓶:250ml。
试剂和溶液
- 浓硫酸:不含氮。
- 无氨的水:按GBT 603-2002 化学试剂 试验方法中所用制剂及制品的制备制备。
- 混合催化剂:将硫酸钾(K2SO4)100g、二氧化钛(TiO2)3g和硫酸铜(CuSO4·5H2O)3g混合并研细。
- C.5.3.4.氢氧化钠溶液(450g/L):称取氢氧化钠450g,溶解于1L水中。用一个带盖的不锈钢杯加热煮沸,以排除氨。冷却,让其不溶物沉淀。将上清液移入一个带胶塞的塑料瓶贮存,此溶液相对密度应不低于1.35.
- 锌粒。
- C.5.3.6.硼酸溶液(2g/L):称取20g硼酸,用水溶解,并定容至1L。
- C.5.3.7.盐酸标准滴定溶液(c(HCl)=0.1mol/L):按GBT 601-2002 化学试剂 标准滴定溶液的制备配制与标定。
- 溴甲酚绿指示液:按GBT 603-2002 化学试剂 试验方法中所用制剂及制品的制备配制。
分析步骤
成套仪器按使用说明书进行试样的测定。自行组装的仪器按下述方法进行操作。
- 消化
- 吸取试样(4.1)25ml置于凯氏烧瓶(或消化管)内,在通风橱中,加入2ml浓硫酸,浓缩至黏稠。加入混合催化剂10g、浓硫酸25ml,轻轻摇动混合均匀。将凯氏烧瓶斜放在加热器的支架上,加热至不再发泡时,提高温度变化。待溶液清亮后再消化30min(或使用凯氏定氮分析仪专门的消化管消化)。将消化液冷却至室温。
- 蒸馏
- 待消化液冷却后,缓缓加入无氨的水250ml,摇匀,冷却,并加入少许锌粒。连接凯氏烧瓶与蒸馏装置,馏出管的尖端插入已盛有25ml硼酸溶液(C.5.3.6)和0.5ml溴甲酚绿混合指示液的三角瓶中,馏出管尖端应在液面之下。通过加液漏斗加入70ml氢氧化钠溶液(C.5.3.4)于凯氏烧瓶中,轻轻摇匀,使内容物混匀,然后加热蒸馏。等馏出液达到180ml时,停止蒸馏。
- 滴定
- 用盐酸标准滴定溶液(C.5.3.7)滴定馏出液,当溶液由绿色消失转变为灰紫色即为终点。记录消耗盐酸标准滴定溶液的体积(V11)。
- 同时,按上述方法做空白试验,记录消耗盐酸标准滴定溶液的体积(V10)。
结果计算
精密度
重复性误差的变异系数1.9%;再现性误差的变异系数3.9%。
总多酚
原理
在碱性溶液(pH=10~12)中,多酚类物质与三价铁生成较稳定的红色化合物,颜色深浅与多酚类物质含量成正比,用分光光度计测定。
仪器
- 分光光度计:备有10mm比色皿。
- 离心机。
- 比色管:25ml、50ml。
试剂和溶液
- 羧甲基纤维素钠-乙二胺四乙酸二钠溶液(CMC-EDTA):在500ml水中慢慢加入纯羧甲基纤维素钠10.0g和乙二胺四乙酸二钠2.0g,边加边搅拌,待全部溶解后,停止搅拌,静置1h~3h,全部移入1L容量瓶中并定容。必要时,可用离心机离心,使溶液澄清。该溶液每月需重新配置。
- 铁试剂:称取绿色柠檬酸铁铵(Fe(NH4)3(C6H5O7)2)3.5g,加水溶解并定容至100ml。该溶液应完全澄清,每周(或更短时间)配制一次。
- 氨试剂:氨水+水=1+2。
分析步骤
空白管:吸取试样(按4.1除气但未过滤的,20℃啤酒)10ml与25ml容量瓶中,加入8ml CMC-EDTA溶液,充分混匀,加入0.5ml氨试剂,混匀。用水定容,摇匀。放置10min后,用10mm比色皿,在波长600nm下,测定其吸光度。
试样管:吸取试样(按4.1除气但未过滤的,20℃啤酒)10ml与25ml容量瓶中,加入8ml CMC-EDTA溶液,充分混匀,加入0.5ml铁试剂,混匀。然后加入0.5ml氨试剂,混匀。用水定容,摇匀。放置10min后,以空白管做参比液,用10mm比色皿,在波长600nm下,测定其吸光度。
试样的稀释:若总多酚超过400mg/L,试样就需要稀释。试样和空白都用50ml容量瓶。在取样、添加了CMC-EDTA溶液和铁试剂后,加水25ml,充分混匀,再加氨试剂,用水定容,摇匀。
结果计算
精密度
总多酚含量为180mg/L时,重复性误差的变异系数3%;再现性误差的变异系数6%。 注1:啤酒试样应澄清透明,否则就需要通过离心方法使之完全澄清透明(但不能用过滤法);注意离心也会除去一些已沉淀的多酚物质,使老化啤酒测试结果偏低。为此,对于轻度浑浊啤酒,可用等体积水稀释,以增加其透明度。
注2:在测定过程中,不论是试样还是空白,每加一种试剂后,都要充分摇匀,再加下一种试剂。
铁
比色法
- 原理
- 在pH=3~9条件下,低价铁离子与邻菲罗啉生成稳定的橘红色络合物,其色度与二价铁的含量成正比,在波长505nm下,有最大吸收。
- 仪器
- 分光光度计:备有10mm比色皿。
- 恒温水浴:控温精度±0.5℃。
- 移液管:1.0ml、2.0ml、5.0ml、10.0ml、20.0ml、25.0ml、50.0ml。
- 容量瓶:100ml、500ml。
- 具塞比色管:50ml。
- 试剂和溶液
- 显色剂:称取邻菲罗啉1.50g,加200ml水加热至70℃溶解,并用水定容至500ml。
- 铁标准贮备液(0.1mg/ml):按GBT 602-2002 杂质测定用标准溶液的制备。
- 铁标准使用液(10μg/ml):吸取铁标准贮备液10.0ml于100ml容量瓶中,用水定容。
- 抗坏血酸:不含铁,研成细粉。
- 分析步骤
- 绘制标准工作曲线
- 分别吸取帖标准使用液0.0ml、2.0ml、5.0ml、10.0ml、20.0ml、30.0ml于6个100ml容量瓶中,加水定容、即得到分别为0mg/L、0.20mg/L、0.50mg/L、1.00mg/L、2.00mg/L、3.00mg/L铁标准溶液。分别吸取所配成的铁标准溶液各25ml于6支50ml具塞比色管中,各加25mg抗坏血酸和2ml显色剂,混合均匀,置于60℃±0.5℃水浴恒温15min。然后取出,迅速冷却至室温。在波长505nm下,以水作参比液。测定其吸光度。用吸光度与对应的铁含量绘制标准曲线(或建立回归方程)。
- 测定
- 吸取两份试样(按4.1除气但未过滤的,20℃啤酒)25.0ml,分别置于两支50ml具塞比色管A、B中。于比色管A中,加25mg抗坏血酸和2ml显色剂,混合均匀,于比色管B中,加25mg抗坏血酸和2ml水,混合均匀,同时将比色管A、B置于60℃±0.5℃水浴恒温15min。然后取出,迅速冷却至室温。在波长505nm下,以B管作参比,测定比色管A中溶液的吸光度,从标准曲线上查得其铁含量(或用回归方程计算)。
- 精密度
- 试样中铁含量为0.20ml/L时,重现性误差的变异系数为10%,再现性误差的变异系数为40%。
原子吸收分光光度法
- 原理
- 啤酒中的铁直接导入原子吸收分光光度计中,在火焰中被原子化,基态原子铁吸收特征波长(248.3nm)的光,吸收量的大小与铁含量成正比,测其吸光度,求得铁含量。
- 该法局限于直接吸收灵敏度为0.05mg/L水平的仪器,而且应采用标准加入法(增量法)测定。
- 仪器
- 原子吸收分光光度计:备有铁空心阴极灯。
- 容量瓶:100ml。
- 刻度移液管:1ml,分度值0.1ml。
- 移液管:10ml。
- 分析天平:感量0.1mg。
- 试剂和溶液
- 硝酸溶液:浓硝酸+水=1+1;
- 铁标准贮备液(1000mg/L):称取纯铁丝1.000g(精确至0.1mg),溶于50ml硝酸溶液中,用水稀释至1L(或使用商品铁标准溶液)。
- 分析步骤
- 试样标准溶液的配置
- 吸取铁标准贮备液100ml,用水稀释至1000ml,该铁标准溶液浓度为100ml/L。
- 分别吸取100mg/L铁标准溶液0.00ml、0.10ml、0.20ml、0.40ml、0.60ml于5个100ml容量瓶中,用试样(按4.1除气但未过滤的,20℃啤酒。如需过滤时,应用无铁滤纸)稀释至刻度。
- 测定
- 选择适宜的操作条件,先用空白溶液在波长248.3nm处调节仪器零点。再分别导入啤酒标准溶液,测定其吸光度,以标准溶液浓度为横坐标,以相对应的吸光度为纵坐标,绘制标准工作曲线。用外插法,将标准曲线反向延长与横轴相交,交点(X)即为待测啤酒试样的铁含量(或建立回归方程计算)。
- 所得结果表示至两位小数。
- 精密度
- 试样中铁含量为0.30mg/L时,重现性误差的变异系数为8%,再现性误差的变异系数为17%。
低沸点香味成分
原理
啤酒中低沸点的醇、酯类物质,采用顶空进样,用配有FID检测器的气相色谱仪测定,用内标法定量。
仪器
- 气相色谱仪:配有FID检测器。
- 毛细管色谱柱:PEG 20M 30m×0.53mm,图层1μm(或使用同等分析效果的柱子)。
- 顶空取样瓶:20ml,带密封垫及铝压盖。
- 注射器:2ml压力密闭,气密。
- 恒温水浴:控温精度±0.5℃。
- 恒温干燥箱。
试剂和溶液
- 正丁醇内标贮备液:称取正丁醇20g,用95%乙醇溶解并定容至100ml。冷藏可保存1个月~2个月。
- 正丁醇内标使用液:使用时,吸取正丁醇内标贮备液1.00ml,用水稀释至100ml,混匀。
- 香味成分混合标准贮备液:分别称取标准样品乙酸乙酯4g、正丙醇2g、异丁醇2g、乙酸异戊酯0.5g、异戊醇7.5g,用95%乙醇溶解并定容至100ml。冷藏可保存1个月~2个月。
分析步骤
- 试样的制备
- 于20ml顶空取样瓶中,加入至少在0℃冷却12h的试样10.0ml,再向其中加入100μL内标使用液,用铝压盖密封。
- 测定
- 色谱条件:
- 进样口温度:200℃;
- 检测器温度:200℃;
- 柱温:40℃保温5min,然后以10℃/min程序升温至140℃,再保温3min;
- 载气(高纯氮)流量:5ml/min。
- 将装有试样的顶空取样瓶放入40℃±0.5℃恒温水浴中保温45min,使气液两相达到平衡状态。用预先在恒温箱保温至40℃的注射器插入顶空取样瓶的气相中,反复抽洗5次,然后抽取1.00ml进入色谱仪,记录色谱图。
- 绘制标准曲线
- 用4%乙醇溶液稀释香味成分混合标准贮备液,制成两种标准使用溶液。使其中的乙酸乙酯、正丙醇、异丁醇、乙酸异戊酯和异戊醇浓度分别为4mg/L、2mg/L、2mg/L、0.5mg/L、7.5mg/L和40mg/L、20mg/L、20mg/L、5mg/L、75mg/L。按试样测定作同样的操作,测量各组份色谱峰和内标峰峰面积,反复测定三次,取平均值,以内标法绘制标准曲线(或建立回归方程计算)。
- 所得结果表示至一位小数。
精密度
各种组分含量在40mg/L时,再现性误差的变异系数约为4%~8%。
双乙酰(气相色谱法)
原理
试样进入气相色谱仪中的色谱柱时,由于在气液两相中分配系数不同,而使双乙酰、2,3-戊二酮、2,3-己二酮及其他组分得以完全分离。利用电子捕获检测器捕获低能量电子,而使基流下降产生信号,与标样对照,根据保留时间定性,利用内标法或外标法定量。进入色谱柱前不经过加热处理,测得的是游离连二酮;于60℃加热90min后,测得的是包括前驱体转化在内的总连二酮。
仪器
- 气相色谱仪:配有ECD检测器。
- 微量注射器:2ml压力封闭,气密。
- 顶空取样瓶:20ml,带密封垫及铝压盖。
- 恒温水浴:控温精度±0.5℃。
- 恒温干燥箱。
- 分析天平:感量0.1mg。
试剂和溶液
- 2,3-己二酮(2,3-hexanedione):
- 内标贮备溶液:称取2,3-己二酮500mg(精确至0.1mg),用水溶解,并定容至100ml。该溶液在冷藏条件下可稳定1个月~2个月;
- 内标使用溶液:吸取内标贮备溶液1.00ml,置于100ml容量瓶中,用水稀释至刻度。该溶液需当天用当天配。
- 2,3-戊二酮(2,3-pentanedione):标准贮备溶液和标准使用溶液的配制方法同上述2,3-己二酮。
- 双乙酰(diacetyl):标准贮备溶液和标准使用溶液的配制方法同上述2,3-己二酮。
- 氯化钠。
色谱柱与色谱条件
- 色谱柱
- 填充柱:不锈钢(或玻璃)柱2m。固定相:在Chrornosorb WAW-DMS上,涂以10%聚乙二醇-20M(PEG-20M);或在Carbopak C上,涂以0.2%聚乙二醇-1500(PEG-1500)。
- 毛细管色谱柱:固定相为Carbowax 20M。
- 或者选用同等分析效果的其他色谱柱。
- 色谱条件
- 柱温:55℃;
- 汽化室温度:150℃;
- 检测器温度:200℃;
- 载气(高纯氮)流量:25ml/min。
- 应根据不同仪器,通过试验选择最佳色谱条件,以使2,3-戊二酮、2,3-己二酮和双乙酰获得完全分离为准。
分析步骤
- C.9.5.1.标准溶液的制备
- 在顶空取样瓶中装入水10ml和氯化钠4g,加入2,3-戊二酮、2,3-己二酮和双乙酰三种标准使用溶液各10μL,用衬有密封垫铝压盖卷边密封。用手摇匀50s。该溶液所含三种标准物质的浓度各为0.05mg/L。
- 若预计扩大线性响应范围连二酮(VDKs)含量0.05mg/L时,应适当调整标准溶液的浓度(如0.10、0.15、0.20mg/L),使响应值成线性。
- C.9.5.2.试样的制备
- 啤酒样品的游离连二酮(VDKs)
- 取室温下的啤酒样品,缓慢倒入刻度试管中,用吸管吸去泡沫及多余的酒液只10ml。
- 于20ml顶空取样瓶中,移入啤酒样10ml、加氯化钠4g和内标(2,3-己二酮)使用溶液10μL,用铝压盖密封。用手摇匀50s。
- 啤酒样品的总连二酮(VDKs+前驱体)
- 在400ml烧杯中,取啤酒样100ml,轻轻摇动脱气。然后通过两个杯子缓慢注流倒杯5次,使其很好曝气。缓缓倒入刻度试管中,用吸管吸取泡沫及多余的酒液,使试管中的酒样为10ml,将其移入装有4g氯化钠的20ml顶空取样瓶中,加入内标(2,3-己二酮)使用溶液10μL,用铝压盖密封。
- 于60℃水浴中保温90min。冷却至室温后,轻轻拍打瓶盖使盖残留的液滴落下。用手摇匀50s。
- 测定
- 标准溶液的测定
- 将标准溶液(C.9.5.1)放入30℃水浴中保温30min,使气相达到平衡状态。置于自动进样器上进样1.0ml,记录2,3-戊二酮、2,3-己二酮和双乙酰峰的保留时间和逢高(或峰面积)。根据峰的保留时间定性。根据逢高(或峰面积),求得校正因子进行定量。作校正因子时,应反复进样分析三次,取平均值计算。
- 试样的测定
- 将制备好的试样(C.9.5.2)放于30℃水浴中保温30min,使气相达到平衡状态。置于顶空自动进样器上进样1.0ml(或将气体注射器插入试样瓶或标样瓶的评定空气中,反复抽吸5次“冲洗”注射器,然后抽取1.0ml注入色谱仪中),在选择好的色谱条件下进行分析。
- 注:在色谱仪器分析时间,应将注射器针管拆开,置于40℃的恒温干燥箱中。
计算结果
精密度
在重复性条件下获得的两次独立测定结果的绝对差值不得超过算术平均值的10%。